客户论文精选|肿瘤滞留型脂质纳米粒-微针系统共递送 SARS-CoV-2 信使核糖核酸与吲哚菁绿用于浅表肿瘤的协同免疫光热治疗
来源:
|
作者:锐视医疗
|
发布时间: 2026-03-05
|
293 次浏览
|
🔊 点击朗读正文
❚❚
▶
|
分享到:
复旦大学赵栋教授团队,近日在国际权威期刊《International Journal of Biological Macromolecules》(IF:8.5)发表论文,题为《Tumor-retained lipid nanoparticle-microneedle systems for codelivery of SARS-CoV-2 mRNA and indocyanine green for synergistic immuno-photothermal therapy of superficial tumors》的研究成果。锐视科技的小动物活体成像系统(IMAGING 200)在研究中被用以动态追踪与定量分析药物在体内的分布规律,直接验证肿瘤滞留型脂质纳米颗粒-微针(LNP-MN)系统的靶向优势。
复旦大学赵栋教授团队,近日在国际权威期刊《International Journal of Biological Macromolecules》(IF:8.5)发表论文,题为《Tumor-retained lipid nanoparticle-microneedle systems for codelivery of SARS-CoV-2 mRNA and indocyanine green for synergistic immuno-photothermal therapy of superficial tumors》的研究成果。锐视科技的小动物活体成像系统(IMAGING 200)在研究中被用以动态追踪与定量分析药物在体内的分布规律,直接验证肿瘤滞留型脂质纳米颗粒-微针(LNP-MN)系统的靶向优势。

该研究首次将SARS-CoV-2 spike mRNA与ICG介导的光热疗法(photothermal therapy,PTT)联合应用于浅表肿瘤治疗,在4 T1乳腺癌模型中,该联合策略取得了显著的肿瘤生长抑制效果(75.1%),增强CD 8 + T细胞浸润,并使全身毒性最小化,这项研究开创了PTT和基于mRNA的肿瘤标记免疫疗法在微创MN平台中的整合,为增强浅表癌症治疗提供了有前途的策略。
IML/MNs 为 10×10 阵列的双层结构锥形微针,上层载有 IML,下层为 PVP 基底,微针尺寸及表面形貌经扫描电镜表征(图6A、6B)。IML 载入微针后,多分散指数与包封率稳定,粒径、表面电荷小幅变化,细胞表达略有下降。体外热稳定性显著优于 IML 溶液,印证脱水可提升 mRNA/LNP 储存稳定性。微针封口膜穿透深度为 393.54±23.95μm,具备皮肤穿透能力;其穿透率随介质厚度增加骤降,252μm 厚度下穿透率 100%,756μm 时完全无法穿透(图 6C)。离体猪皮实验中,微针1分钟溶解近 50%,2 分钟溶解达 80%(图 6D)。光热性能测试表明,近红外照射下,载药微针体外可快速升温至 60℃,空白微针无光热效应;体内实验中,载药微针处理的肿瘤光照后升温至 50℃,与对照组差异显著(图 6E、6F)。采用 Cy7 标记胆固醇示踪荷瘤小鼠体内 IML 分布:静脉注射组荧光信号集中于上腹部,肿瘤无明显信号;微针处理组信号主要富集于肿瘤,仅存在少量淋巴途径的全身渗漏(图 6G)。AUC 定量分析证实瘤内注射 IML/MNs 分布特性优异。给药 24 小时后主要器官定量检测显示:静脉注射组药物主要富集于肝(68.1%)、脾(15.6%),肿瘤蓄积仅 3.1%;瘤内注射微针组肿瘤药物分布达 48.4%,肝脏渗漏降至 23.7%。相较静脉给药,瘤内微针给药使肿瘤药物蓄积提升 15.6 倍,肝脏分布减少 65.2%(图 6H、6I)。
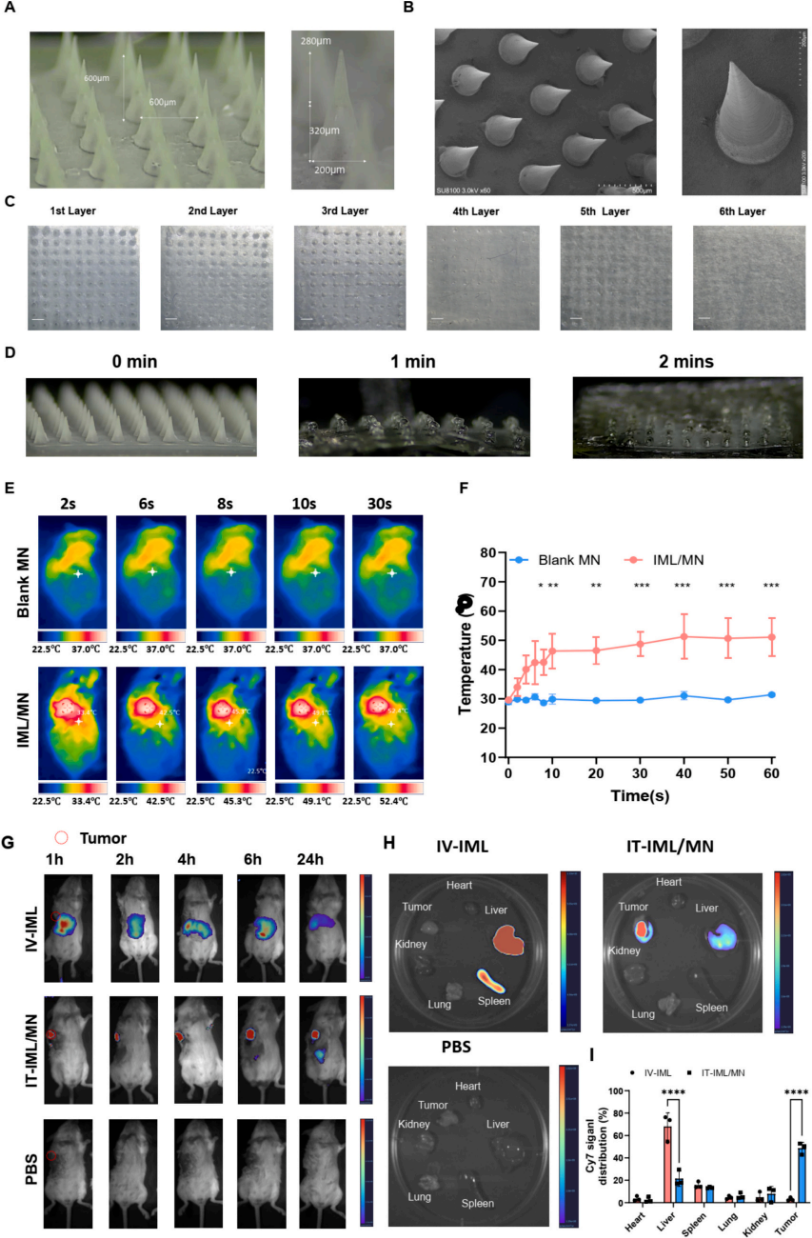
图6. IML/MN的表征和生物分布。IML/MN的显微镜图像(A)和SEM图像(B)。(C)MN处理后Parafilm膜的显微镜图像,比例尺600μm。(D)在猪皮肤中施用2分钟后IML/MN的显微图像。(E)用IML/MN处理的4只T1荷瘤小鼠的热成像和(F)温度-时间曲线。(G)通过i. v.注射施用顶L或通过i.t.注射施用IML/MN的小鼠的发光成像,n = 3.施用后24小时,主要器官和肿瘤中的顶L的生物分布(H)和定量(I)。
▲二维光学活体成像系统(型号:IMAGING 200)DOI: 10.1016/j.ijbiomac.2025.149038